Warum schlanke Menschen krank und vermeintlich Übergewichtige gesund sein können
Eine klinisch-narrative Auseinandersetzung mit dem TOFI-Phänotyp, ektoper Fettdeposition und der Evidenz hinter „metabolischen Biohacks“
Vorbemerkung
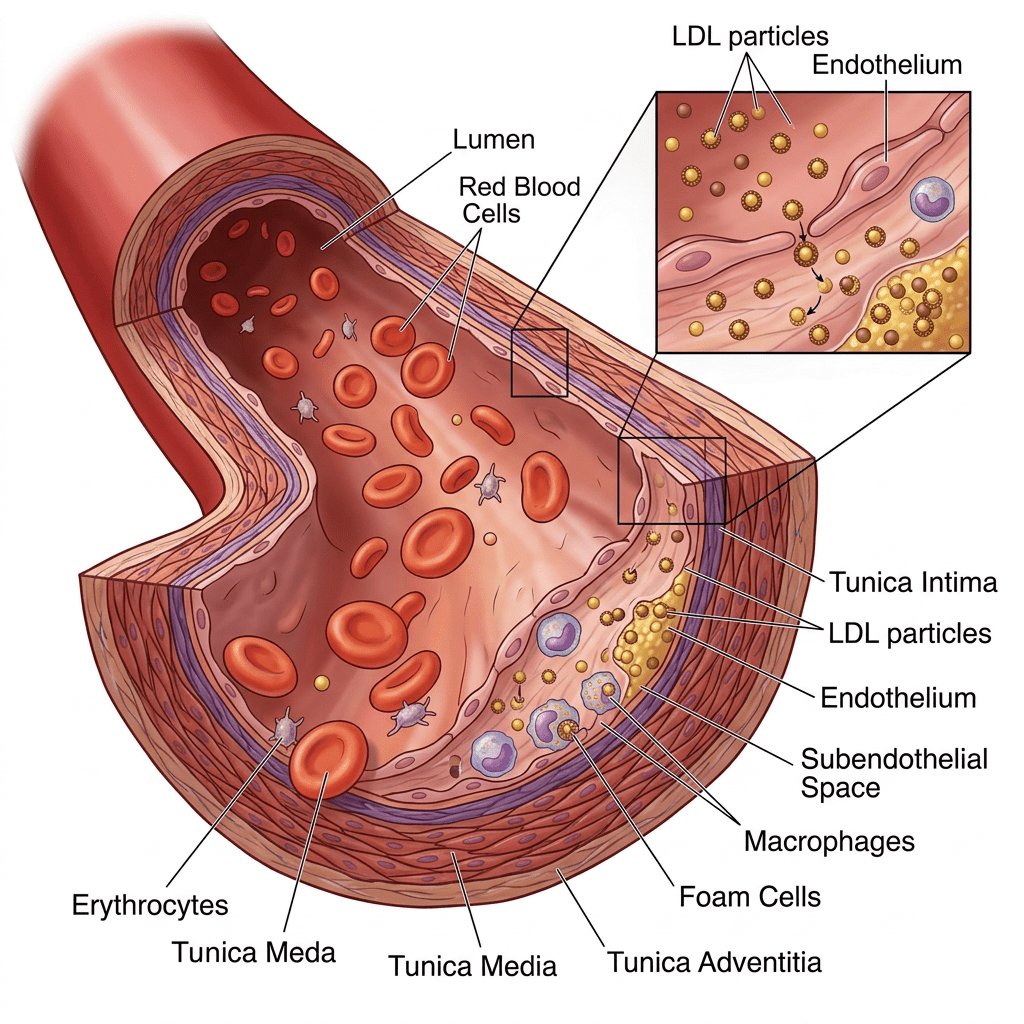
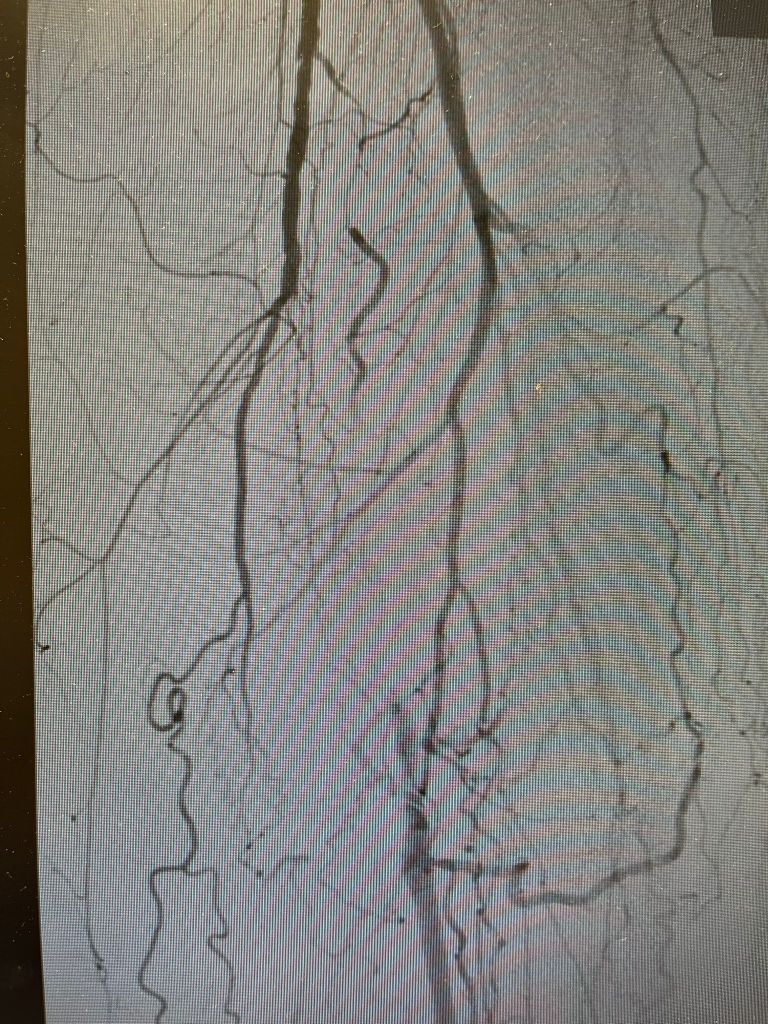
In der Sprechstunde sehe ich regelmäßig Patienten, die mir mit einer gewissen Selbstverständlichkeit erklären, sie seien „eigentlich gesund“ – schlank, sportlich, ernähren sich vernünftig. Dann zeigt das Duplexsonogramm eine Plaque, die Laborkonstellation eine atherogene Dyslipidämie und der Sonografiebefund der Leber eine Steatose, die in dieser Konstellation niemand erwartet hätte. Genau diese Diskrepanz zwischen äußerem Erscheinungsbild und innerer Biologie ist das Thema dieses Beitrags.
Der populäre Begriff „TOFI“ – Thin Outside, Fat Inside – fasst dieses Phänomen griffig zusammen. Wissenschaftlich präziser sprechen wir vom metabolisch obesen Normalgewichtigen (MONW), vom „lean NAFLD“-Phänotyp oder, in der Sprache der modernen Hepatologie, von der schlanken MASLD. Dahinter steht ein gemeinsames pathophysiologisches Prinzip: der Verlust metabolischer Flexibilität. Dieser Beitrag versucht, das Konzept nüchtern darzustellen, die diagnostischen Werkzeuge zu ordnen und die populären Interventionen – Time-Restricted Feeding, Bewegungstiming, postprandiale Spaziergänge – an den verfügbaren Evidenzgrad zurückzubinden.
1. Was metabolische Flexibilität wirklich bedeutet
Der Begriff „metabolische Flexibilität“ wird im Wellness-Diskurs inzwischen so beliebig verwendet, dass seine ursprüngliche Bedeutung zu verschwimmen droht. Geprägt wurde er um die Jahrtausendwende von Kelley und Mandarino [1]. Sie beschrieben damit die Fähigkeit der Skelettmuskulatur, je nach Substratangebot und energetischem Bedarf flexibel zwischen Glukose- und Fettsäureoxidation zu wechseln. Gemessen wird diese Eigenschaft klassisch am respiratorischen Quotienten (RQ) im Wechsel zwischen Nüchtern- und insulinstimuliertem Zustand unter euglykämischer hyperinsulinämischer Clamp.
Ein metabolisch flexibler Muskel oxidiert nüchtern überwiegend Fettsäuren (RQ um 0,7) und schaltet unter Insulinstimulation rasch auf Glukoseoxidation um (RQ in Richtung 1,0). Die Differenz – ΔRQ – ist das eigentliche Maß. Beim insulinresistenten, „metabolisch starren“ Muskel ist diese Differenz verkleinert: Er oxidiert nüchtern bereits zu viel Glukose und kann unter Insulin nicht mehr adäquat hochfahren.
Continuous Glucose Monitoring (CGM), wie es heute durch Geräte wie das FreeStyle Libre oder den Dexcom verfügbar ist, misst diese Flexibilität nicht direkt. Was CGM zeigt – postprandiale Exkursionen, nächtliche Stabilität, glykämische Variabilität (ausgedrückt etwa als MAGE oder Coefficient of Variation) – sind Surrogatparameter. Sie korrelieren mit metabolischer Flexibilität, sind aber nicht mit ihr identisch. Diese Unterscheidung ist wichtig, weil sich daraus die Grenzen der Selbstvermessung ergeben: Ein CGM zeigt, wie der Körper auf eine Mahlzeit reagiert. Es zeigt nicht, ob der Muskel die Substratwahl im Wechsel der Tageszeiten und Belastungszustände sauber regelt.
2. Der TOFI-Phänotyp – eine klinische Annäherung
Der Begriff TOFI wurde wissenschaftlich vor allem durch die Arbeitsgruppe um Jimmy Bell und E. Louise Thomas am Imperial College London geprägt [2]. Mittels Magnetresonanz-Bildgebung zeigte die Gruppe, dass eine erhebliche Zahl normalgewichtiger Probanden ein viszerales Fettvolumen aufweist, das dem deutlich übergewichtiger Vergleichspersonen entspricht. Der entscheidende Befund: Die externe Anthropometrie – Body-Mass-Index, sogar der Bauchumfang in unauffälligen Bereichen – versagt bei der Detektion dieses Phänotyps.
2.1 Begriffsklärung
In der Literatur kursieren mehrere Bezeichnungen, die nicht ganz deckungsgleich sind:
- Metabolically Obese Normal Weight (MONW): Stammt aus der Arbeit von Ruderman et al. [3] und beschreibt normalgewichtige Personen mit Hyperinsulinämie und atherogener Dyslipidämie.
- Lean NAFLD / lean MASLD: Hepatologisch definierter Subtyp mit Lebersteatose bei BMI < 25 kg/m² (Asien: < 23 kg/m²). Wird zunehmend als eigene Entität beschrieben [4].
- TOFI: Bildgebungsbasierter Begriff mit Fokus auf viszerales und ektopes Fett.
Diese Begriffe überlappen, sind aber nicht synonym. Ein lean NAFLD-Patient hat nicht zwingend erhöhtes viszerales Fett (intrahepatische Steatose kann auch ohne ausgeprägte viszerale Adipositas auftreten), ein MONW-Patient nicht zwingend eine Steatohepatitis.
2.2 Genetische Determinanten
Die Vorstellung, schlanke metabolische Erkrankung sei rein lebensstilbedingt, greift zu kurz. Bei lean NAFLD finden sich gehäuft Risikoallele in PNPLA3 (rs738409 G), TM6SF2 und MBOAT7 [5]. Diese Varianten erklären, warum manche Patienten trotz unauffälliger Lebensführung intrahepatische Triglyzeride akkumulieren – ein Punkt, den ich in der Aufklärung gerne explizit anspreche, weil er den oft moralisch aufgeladenen Diskurs um „Eigenverschulden“ entschärft.
3. Ektope Fettdeposition – wo das Fett wirklich Schaden anrichtet
Wenn die subkutane Fettdepotkapazität individuell überschritten wird – sei es durch positive Energiebilanz, sei es durch ein genetisch limitiertes subkutanes Reservoir –, beginnt der Körper, Fett an Orten einzulagern, an denen es funktionell nichts verloren hat. Diese ektope Fettdeposition ist der eigentliche Treiber der metabolischen Pathologie [6].
3.1 Viszerales versus retroperitoneales Fett
In populären Texten wird häufig pauschal vom „Bauchfett“ gesprochen, das die Organe „umgibt“. Anatomisch und pathophysiologisch sollten wir genauer sein. Das klassische viszerale Fett ist intraperitoneal lokalisiert – omental und mesenterial – und drainiert über die Pfortader direkt zur Leber. Das ist der Grund, warum es so eng mit Lebersteatose und systemischer Insulinresistenz verknüpft ist: Freie Fettsäuren und Adipokine erreichen die Leber in „erster Passage“.
Das perirenale und retroperitoneale Fett dagegen drainiert nicht über die Pfortader. Es wird in der aktuellen Literatur zunehmend als eigenständig metabolisch aktives Depot beschrieben, korreliert mit Hypertonie und chronischer Niereninsuffizienz [7], ist aber pathophysiologisch nicht mit dem omental-mesenterialen Fett gleichzusetzen.
3.2 Organspezifische Konsequenzen
Die Folgen ektoper Fettdeposition sind organspezifisch:
- Leber: Hepatozytäre Triglyzeridakkumulation → MASLD/MASH → Fibrose; gleichzeitig hepatische Insulinresistenz mit gestörter Suppression der hepatischen Glukoseproduktion.
- Pankreas: Inselzell-Lipotoxizität mit gestörter Erstphasen-Insulinsekretion. Taylor und Mitarbeiter haben in der DiRECT-Studie gezeigt, dass diese Veränderungen reversibel sind, sobald der intrapankreatische Fettgehalt durch Gewichtsreduktion sinkt [8].
- Skelettmuskel: Intramyozelluläre Lipide (IMCL) – allerdings paradox: Auch trainierte Ausdauersportler zeigen erhöhte IMCL bei intakter Insulinsensitivität („Athleten-Paradoxon“). Entscheidend ist nicht die Menge, sondern die Qualität – das Verhältnis von Diacylglycerolen und Ceramiden zu neutralen Triglyzeriden [9].
- Herz: Epikardiales Fett ist eigenständiger kardiovaskulärer Risikomarker, unabhängig vom BMI [10].
- Gefäße: Perivaskuläres Fett moduliert lokal die Endothelfunktion und plaque-Biologie – ein Aspekt, der für die Gefäßmedizin von wachsender Bedeutung ist.
4. Diagnostik – ein abgestuftes Vorgehen
Wer den TOFI-Phänotyp diagnostizieren will, muss über BMI und Bauchumfang hinausgehen. Sinnvoll ist ein Stufenschema.
4.1 Stufe 1 – einfache Laborchemie
- Nüchtern-Triglyzeride und HDL-Cholesterin: Eine erhöhte TG/HDL-Ratio ist einer der robustesten Surrogatmarker peripherer Insulinresistenz [11].
- Nüchterninsulin und HOMA-IR: HOMA-IR = (Insulin µU/mL × Glukose mg/dL) / 405. Werte > 2,5 gelten als hinweisend, > 3,5 als deutlich pathologisch – wobei die Schwellen laborabhängig variieren.
- ApoB: Inzwischen verlässlicherer kardiovaskulärer Risikomarker als LDL-Cholesterin allein, insbesondere bei TG-Erhöhung mit small-dense-LDL.
- HbA1c plus Nüchternglukose: Detektiert manifesten Diabetes, ist aber für frühe Insulinresistenz zu unsensitiv.
4.2 Stufe 2 – funktionelle und Bildgebung
- Oraler Glukosetoleranztest mit Insulinmessung: Erfasst postprandiale Hyperinsulinämie früher als HbA1c.
- Lebersonografie: Erste Stufe zur Erfassung einer Steatose; ergänzt durch transiente Elastografie (FibroScan mit CAP) zur Quantifizierung.
- MR-Spektroskopie / MR-PDFF: Goldstandard für hepatischen Fettgehalt, in Studien zunehmend Standard.
- DEXA: Erlaubt regionale Fettverteilung (android/gynoid Ratio, viszerales Fett) jenseits einfacher Anthropometrie.
4.3 Stufe 3 – kontinuierliche Verlaufsmessung
CGM ist in der Frühdiagnostik der Insulinresistenz noch nicht etabliert, aber ein zunehmend interessantes Werkzeug zur individualisierten Verlaufsbeurteilung. Klinisch verwertbare Metriken sind die postprandiale Spitzenglukose, die Zeit oberhalb 140 mg/dL nach Mahlzeiten, die nächtliche Stabilität und der Coefficient of Variation. Ein CV > 36 % gilt bei Diabetikern als Indikator hoher Variabilität – Referenzwerte für Stoffwechselgesunde sind weniger gut etabliert, in der Größenordnung um 15–20 % wird häufig diskutiert.
5. Triglyzerid/HDL-Ratio – ein präzises Wort zu einem populären Marker
Die TG/HDL-Ratio gehört zu den meistdiskutierten Surrogatmarkern der Insulinresistenz. Zwei Punkte werden dabei häufig falsch dargestellt.
Erstens: Die Ratio ist dimensionslos. Wer sie mit der Einheit „mg/dL“ angibt, verwechselt den Quotienten mit dem Zähler. Je nachdem, ob die Ausgangswerte in mg/dL (US) oder mmol/L (Europa) gemessen werden, ändern sich die Cut-offs erheblich, weil der Umrechnungsfaktor für Triglyzeride (88,57) ein anderer ist als für Cholesterin (38,67).
Zweitens: Die häufig zitierten Schwellen – < 2,0 günstig, > 4,0 ungünstig (in mg/dL-Einheiten gemessen) – sind ethnisch nicht universell. Sumner et al. zeigten, dass die Korrelation der TG/HDL-Ratio mit Insulinresistenz bei Personen afrikanischer Abstammung deutlich schwächer ist [12]. Bei dieser Gruppe ist der Marker mit Vorsicht zu interpretieren.
Praktisch verwende ich folgende Orientierung – mit dem expliziten Hinweis, dass es Surrogatwerte sind, keine diagnostischen Kriterien:
- In mg/dL: < 2,0 günstig, 2,0–3,5 Graubereich, > 3,5–4,0 hinweisend auf Insulinresistenz
- In mmol/L: < 0,87 günstig, > 1,5–1,7 hinweisend auf Insulinresistenz
- Bei Kombination mit erhöhtem Bauchumfang, Hypertonie oder Glukose-Auffälligkeiten zunehmend prädiktiv
6. Interventionen – nach Evidenzgrad sortiert
6.1 Gut belegt: Bewegung
Bewegung wirkt auf die Glukosehomöostase über zwei mechanistisch unterschiedliche Wege. Erstens: insulinabhängige GLUT4-Translokation – verbessert nach Training, weil das Trainings-induzierte Mehr an GLUT4-Protein die maximale Glukoseaufnahmekapazität anhebt. Zweitens, und das ist die für die Praxis spannendere Pointe: insulinunabhängige GLUT4-Translokation durch Muskelkontraktion, vermittelt über AMPK [13]. Genau dieser Mechanismus erklärt, warum ein einfacher Spaziergang nach dem Essen die postprandiale Glukoseexkursion abflacht – auch beim insulinresistenten Patienten.
Die Daten zum postprandialen Spaziergang sind methodisch heterogen, aber konsistent in der Richtung: Selbst zwei bis fünf Minuten leichter Bewegung 15–60 Minuten nach einer kohlenhydrathaltigen Mahlzeit reduzieren den glykämischen Peak messbar [14]. Das ist eine der wenigen „Lifestyle-Interventionen“ mit minimaler Aufwand-Nutzen-Relation und einem mechanistisch sauber erklärbaren Effekt.
Strukturelles Training kombiniert sinnvoll Ausdauer- und Krafttraining. Krafttraining führt zu Hypertrophie der bestehenden Muskelfasern – eine echte Faserkonversion zwischen Typ I und Typ II ist umstritten, innerhalb der IIa/IIx-Subtypen ist ein Shift dokumentiert. Wichtiger als die Faser-Typ-Diskussion ist der Effekt auf die GLUT4-Expression und die Mitochondriendichte. Beides verbessert sich unter regelmäßigem Training, beides ist bei Inaktivität reversibel rückläufig.
Bei Ausdauertraining gilt das Crossover-Konzept nach Brooks und Mercier: Mit zunehmender Belastungsintensität verschiebt sich die Substratoxidation von Fett zu Kohlenhydraten. Trainierte Sportler oxidieren bei gleicher absoluter Belastung mehr Fett als Untrainierte – das ist die Substanz hinter dem populären „Zone-2“-Konzept (Inigo San Millán, Peter Attia). Klinisch bedeutet das: Lange, niedrigintensive Einheiten trainieren primär die Fettoxidationskapazität und mitochondriale Funktion, hochintensive Intervalle adressieren die Glukoseverwertungskapazität.
6.2 Moderat belegt: Mittelmeerkost und kalorische Restriktion
Die mediterrane Ernährungsweise ist die am besten belegte Ernährungsform für kardiovaskuläre und metabolische Endpunkte (PREDIMED [15]). Mechanistisch wirkt sie über mehrere Achsen: Verschiebung der Fettsäurezusammensetzung zugunsten einfach- und mehrfach ungesättigter Fettsäuren, hohe Polyphenoldichte, hoher Ballaststoffgehalt und niedrige glykämische Last.
Kalorische Restriktion ohne Mangelernährung verbessert über Gewichtsreduktion praktisch alle Marker des metabolischen Syndroms. Die DiRECT-Studie hat gezeigt, dass selbst manifester Typ-2-Diabetes durch eine strukturierte kalorische Restriktion mit nachfolgendem Gewichtserhalt in einem erheblichen Anteil der Fälle in Remission gebracht werden kann [8]. Der entscheidende Mechanismus ist die Entladung der ektopen Fettdepots in Leber und Pankreas.
6.3 Strittig: Time-Restricted Feeding und Early TRF
Time-Restricted Feeding hat in den letzten Jahren erhebliche Aufmerksamkeit erfahren. Die mechanistisch interessanteste Variante ist eTRF – Early Time-Restricted Feeding mit Eßfenster am Morgen und frühen Nachmittag. Die einflussreiche Arbeit von Sutton, Peterson und Mitarbeitern (Cell Metabolism 2018) untersuchte 8 prädiabetische Männer im 5-wöchigen Crossover-Design: 6-stündiges Eßfenster (8–14 Uhr) versus 12-stündiges Kontrollfenster, isokalorisch [16]. Das Ergebnis: Verbesserte Insulinsensitivität, niedrigerer Blutdruck, reduzierter oxidativer Stress.
Diese Studie wird seither zitiert, als habe sie eine breite klinische Empfehlung begründet. Tatsächlich war sie eine kleine, sorgfältig durchgeführte Pilotstudie. Größere Folgearbeiten zeichnen ein nüchterneres Bild: Liu und Mitarbeiter publizierten 2022 im New England Journal of Medicine die Ergebnisse einer 12-monatigen randomisierten Studie an 139 adipösen Patienten und fanden keinen signifikanten Vorteil von TRF gegenüber kalorischer Restriktion alleine bezüglich Gewichtsreduktion oder metabolischer Marker [17].
Der aktuelle Evidenzstand erlaubt etwa folgende Aussage: TRF ist eine zulässige Strategie zur kalorischen Restriktion, die manchen Patienten praktisch leichter fällt als kontinuierliches Kalorienzählen. Ein eigenständiger circadianer Mechanismus jenseits der Kalorienbilanz ist plausibel, aber klinisch nicht zweifelsfrei belegt. Die populären Versprechungen rund um TRF gehen über die Datenlage hinaus.
6.4 Spekulativ: Fasting Mimicking Diet und einzelne Supplemente
Die Fasting Mimicking Diet (FMD) nach Valter Longo ist ein definiertes 5-Tage-Protokoll mit kalorischer Restriktion auf etwa 750–1100 kcal/Tag, niedrigem Protein- und Kohlenhydratanteil. Die Originaldaten zeigen Verbesserungen kardiometabolischer Marker [18], die Studien sind aber überschaubar und industrienah. Für den Einsatz im Kontext metabolischer Optimierung ist das Verfahren plausibel und wahrscheinlich sicher bei stoffwechselgesunden Erwachsenen, die Evidenzbasis für robuste klinische Empfehlungen reicht jedoch nicht.
7. Kontraindikationen und Vorsicht
Was in Wellness-Beiträgen meist fehlt, gehört in jeden klinisch ernstzunehmenden Text: Welche Personen sollten die hier diskutierten Interventionen nicht oder nur unter Aufsicht durchführen?
- Diabetiker unter Insulin oder Sulfonylharnstoffen: Hypoglykämierisiko unter TRF und längeren Nüchternphasen.
- Schwangerschaft und Stillzeit: Kein Zeitpunkt für kalorische Restriktion oder TRF.
- Aktuelle oder anamnestische Essstörung: Restriktive Ernährungskonzepte können relevante Trigger sein.
- Sarkopenie, Frailty, Kachexie: Kalorische Restriktion ist hier kontraproduktiv; Priorität hat eiweißreiche Ernährung mit Krafttraining.
- Niereninsuffizienz: Hochproteinkost erfordert individuelle Abwägung.
- Schilddrüsenhormone, Bisphosphonate: Resorption ist nüchtern-Fenster-abhängig; TRF erfordert Anpassung der Einnahmezeiten.
8. Zusammenfassung und klinische Praxis
Metabolische Flexibilität ist mehr als ein modischer Begriff. Sie beschreibt eine messbare physiologische Eigenschaft, die im Verlauf eines unmerklichen Prozesses verloren geht – lange bevor Waage, BMI oder Spiegel etwas davon andeuten. Der TOFI-Phänotyp ist klinisch real, betrifft eine relevante Zahl scheinbar gesunder, oft sportlicher Patienten und wird durch konventionelle Anthropometrie nicht erfasst.
Für die klinische Praxis ergibt sich daraus eine pragmatische Stufe: Anamnese und körperliche Untersuchung ergänzt um eine erweiterte Laborchemie (TG/HDL-Ratio, Nüchterninsulin und HOMA-IR, ApoB), bei Auffälligkeit gefolgt von Lebersonografie, gegebenenfalls Elastografie, und – bei wissenschaftlichem oder dokumentarischem Anspruch – DEXA oder MR-PDFF. Therapeutisch ist die Evidenzlage am robustesten für Bewegung (kombiniert Ausdauer und Kraft, ergänzt um postprandiale Aktivität) und für eine mediterran orientierte Ernährungsweise. TRF ist eine zulässige zusätzliche Strategie, kein Wundermittel.
Für den Patienten lautet die Botschaft so: Was im Spiegel zu sehen ist, sagt wenig über die metabolische Innenwelt aus. Wer die richtigen Parameter misst und die richtigen Hebel bedient, kann metabolische Flexibilität erhalten oder zurückgewinnen – ohne Übertreibung, ohne ideologische Aufladung, mit dem ruhigen Handwerkszeug der internistischen und gefäßmedizinischen Tradition.
Literatur
1. Kelley DE, Mandarino LJ. Fuel selection in human skeletal muscle in insulin resistance: a reexamination. Diabetes. 2000;49(5):677–683.
2. Thomas EL, Frost G, Taylor-Robinson SD, Bell JD. Excess body fat in obese and normal-weight subjects. Nutr Res Rev. 2012;25(1):150–161.
3. Ruderman N, Chisholm D, Pi-Sunyer X, Schneider S. The metabolically obese, normal-weight individual revisited. Diabetes. 1998;47(5):699–713.
4. Chrysavgis L, Ztriva E, Protopapas A, Tziomalos K, Cholongitas E. Nonalcoholic fatty liver disease in lean subjects: prognosis, outcomes and management. World J Gastroenterol. 2020;26(42):6514–6528.
5. Romeo S, Kozlitina J, Xing C, et al. Genetic variation in PNPLA3 confers susceptibility to nonalcoholic fatty liver disease. Nat Genet. 2008;40(12):1461–1465.
6. Després JP, Lemieux I. Abdominal obesity and metabolic syndrome. Nature. 2006;444(7121):881–887.
7. Hammoud SH, AlZaim I, Al-Dhaheri Y, Eid AH, El-Yazbi AF. Perirenal Adipose Tissue Inflammation: Novel Insights Linking Metabolic Dysfunction to Renal Diseases. Front Endocrinol. 2021;12:707126.
8. Lean MEJ, Leslie WS, Barnes AC, et al. Primary care-led weight management for remission of type 2 diabetes (DiRECT): an open-label, cluster-randomised trial. Lancet. 2018;391(10120):541–551.
9. Goodpaster BH, Sparks LM. Metabolic Flexibility in Health and Disease. Cell Metab. 2017;25(5):1027–1036.
10. Iacobellis G. Epicardial adipose tissue in contemporary cardiology. Nat Rev Cardiol. 2022;19(9):593–606.
11. McLaughlin T, Reaven G, Abbasi F, et al. Is there a simple way to identify insulin-resistant individuals at increased risk of cardiovascular disease? Am J Cardiol. 2005;96(3):399–404.
12. Sumner AE, Cowie CC. Ethnic differences in the ability of triglyceride levels to identify insulin resistance. Atherosclerosis. 2008;196(2):696–703.
13. Richter EA, Hargreaves M. Exercise, GLUT4, and skeletal muscle glucose uptake. Physiol Rev. 2013;93(3):993–1017.
14. Buffey AJ, Herring MP, Langley CK, Donnelly AE, Carson BP. The Acute Effects of Interrupting Prolonged Sitting Time in Adults with Standing and Light-Intensity Walking on Biomarkers of Cardiometabolic Health: A Systematic Review and Meta-Analysis. Sports Med. 2022;52(8):1765–1787.
15. Estruch R, Ros E, Salas-Salvadó J, et al. Primary prevention of cardiovascular disease with a Mediterranean diet supplemented with extra-virgin olive oil or nuts. N Engl J Med. 2018;378(25):e34.
16. Sutton EF, Beyl R, Early KS, Cefalu WT, Ravussin E, Peterson CM. Early Time-Restricted Feeding Improves Insulin Sensitivity, Blood Pressure, and Oxidative Stress Even without Weight Loss in Men with Prediabetes. Cell Metab. 2018;27(6):1212–1221.e3.
17. Liu D, Huang Y, Huang C, et al. Calorie Restriction with or without Time-Restricted Eating in Weight Loss. N Engl J Med. 2022;386(16):1495–1504.
18. Wei M, Brandhorst S, Shelehchi M, et al. Fasting-mimicking diet and markers/risk factors for aging, diabetes, cancer, and cardiovascular disease. Sci Transl Med. 2017;9(377):eaai8700.
Hinweis: Dieser Beitrag dient der wissenschaftlich-narrativen Aufklärung und ersetzt keine individuelle ärztliche Beratung. Vor Beginn von Ernährungsumstellungen, Trainingsprogrammen oder Time-Restricted-Feeding-Protokollen sollte – insbesondere bei chronischen Erkrankungen oder unter Medikation – ärztliche Rücksprache erfolgen.